Alô, my friend! No blog de hoje, vamos abordar um dos assuntos mais importantes para o Enem e demais vestibulares: a termoquímica! Esse é um conteúdo que aborda, principalmente, as trocas de energia em processos químicos (e, eventualmente, em processos físicos). Pegou papel e cante? Vamos lá?
Só aluno Explicaê Premium tem acesso as provas e gabaritos de vestibulares de todo o Brasil por menos de R$1,35 por dia.

De acordo com as trocas de energia, os processos podem ser divididos em dois tipos: os endotérmicos (que absorvem energia) e os exotérmicos (que liberam energia).
Alguns processos exotérmicos são extremamente importantes, por produzirem energia (respiração, fermentação, combustão):

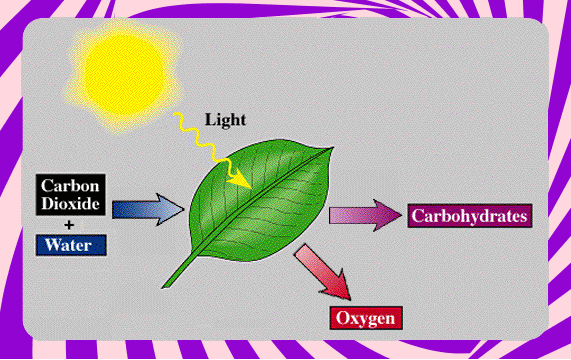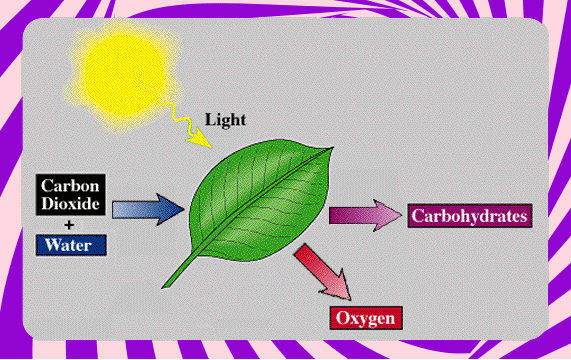
Já nos processos endotérmicos, podemos destacar a fotossíntese:
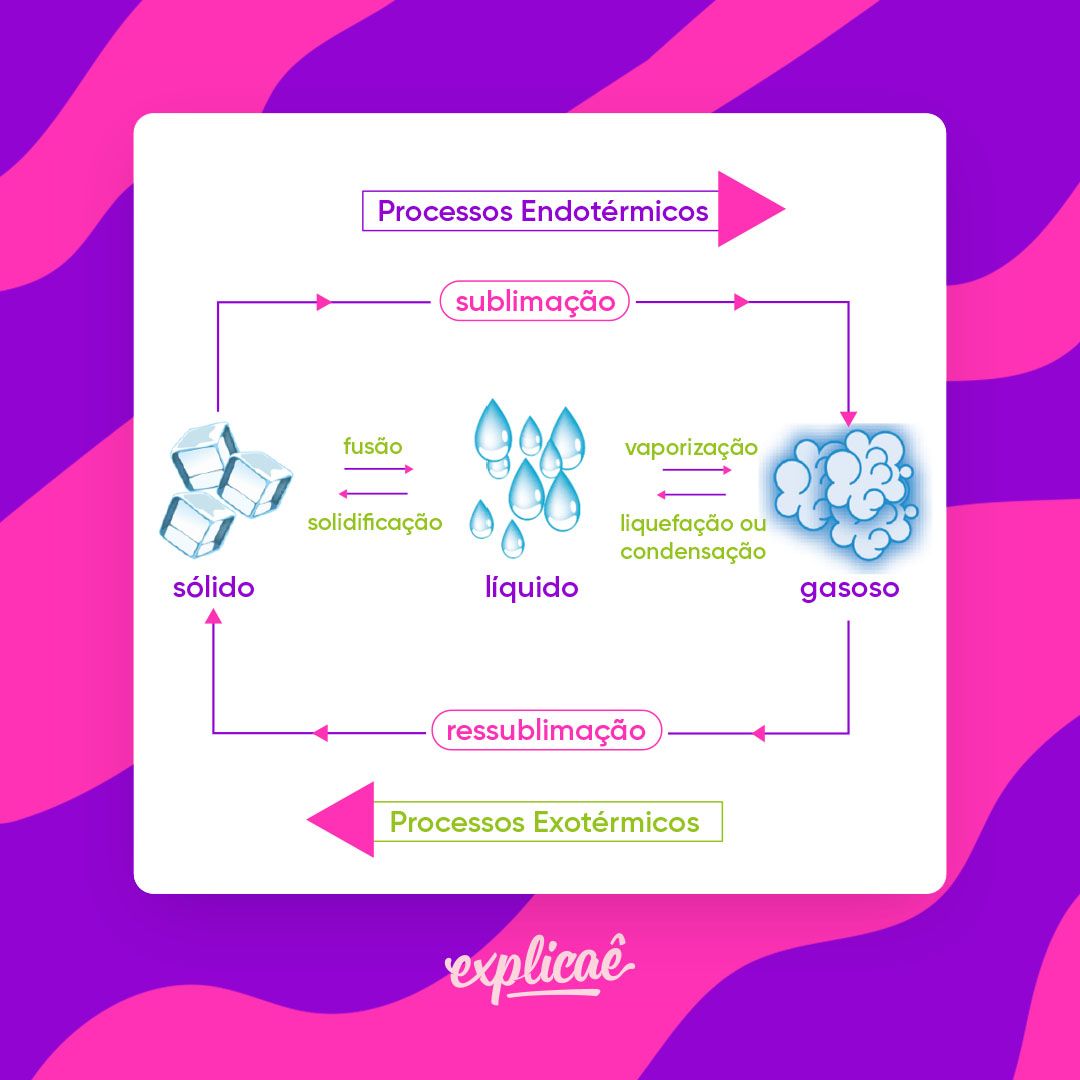
Fique atente porque as provas de vestibulares costumam cobrar as trocas de calor em processos físicos, como as mudanças de estado ilustradas abaixo:
Já os processos químicos (as famosas reações químicas) costumam ser muito mais explorados em provas. Uma forma comum de se medir a energia trocada entre o sistema e o meio ambiente é a entalpia.
Ah, só para que fique claro, entalpia é a energia térmica trocada (ganha ou perdida) quando um processo ocorre em pressão constante (ao ar livre, por exemplo).
Só aluno Explicaê Premium tem acesso a dúvidas ilimitadas por menos de R$1,35 por dia.
De acordo com esta grandeza (entalpia), representada por H (e a sua variação, por DH), temos:
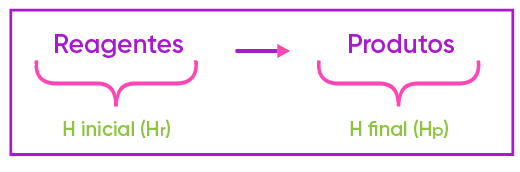
O cálculo do DH
Esse cálculo é feito por Hfinal – Hinicial. Como numa reação, o “final” são os produtos, e o “inicial”, os reagentes. Fica assim:

Para reações endotérmicas, Hfinal > Hinicial,pois ganham energia, e, daí, DH > 0. Já nas reações exotérmicas, ocorre o inverso, pois perdem energia, e DH <0. Os gráficos abaixam ilustram isso.
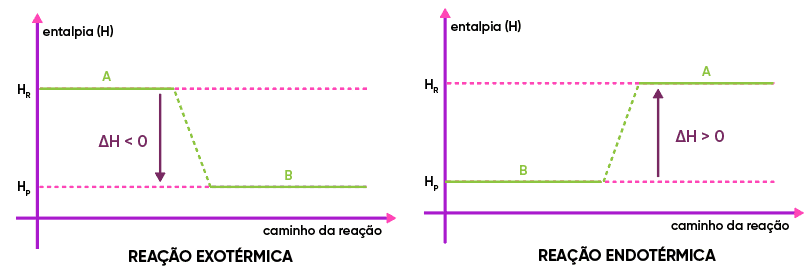
Uma das coisas recorrentes em provas é o cálculo do DH a partir de informações dadas no enunciado. Isso pode ser feito, resumidamente, de quatro formas:
I) Graficamente
Aqui, analisamos o “ponto de partida” (reagentes) e o “ponto de chegada” (produtos). A diferença entre os dois pontos determinará o valor do DH. É importante ressaltar que as reações endotérmicas têm gráfico orientado “para cima” e reações exotérmicas, “para baixo”.

II) Através das entalpias de formação
A entalpias de formação são muito úteis para se determinar o DH de uma reação. Para isso, devemos ter a equação devidamente balanceada e uma tabela com as entalpias de formação de todas as substâncias envolvidas (exceto as substâncias simples no estado-padrão, que, por convenção, têm entalpia zero). O exemplo a seguir mostra isso.
Calcular a entalpia de combustão da glicose, sendo conhecidas as entalpias de formação (em kJ/mol) da glicose (-1268), do gás carbônico (-394) e da água (-286).
Primeiro, escrevemos a equação balanceada:
![]()
Só aluno Explicaê Premium tem correções ilimitadas das suas redações por menos de R$1,35 por dia.
Agora, aplicamos a fórmula DH = Hp – Hr:

(Viu como é fácil? ✌)
III) Através das energias de ligação
Neste caso, precisa-se lembrar de que a quebra de ligações é um processo endotérmico (exige energia para acontecer).

Já o processo inverso (a formação de ligações) libera energia:
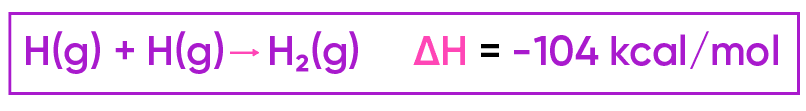
Observe que, neste processo, todas as substâncias devem estar no estado gasoso.
Para calcular, agora, o DH de uma reação, devemos escrever as fórmulas estruturais de todas as substâncias envolvidas, observando as ligações entre seus átomos (preste atenção nas ligações duplas e triplas, se houver, certo, bb?). Então, basta quebrar todas as ligações nos reagentes (absorvendo energia para isso) e formar todas as novas ligações nos produtos (liberando a energia correspondente). O saldo determinará o DH.
Ah, se ligue! Se algumas ligações aparecem repetidas nos reagentes e nos produtos, não precisa quebrá-las (e nem formá-las), certo? Veja no exemplo a seguir:
Determine a variação de entalpia aproximada para a reação abaixo, utilizando as energias de ligação.

Primeiro, vamos escrever as fórmulas estruturais das substâncias:

As ligações em rosa serão quebradas, pois não aparecem no final; em seu lugar, serão formadas novas ligações (em verde). As ligações em pretos não serão alteradas. Então, o DH será dado pela seguinte expressão:
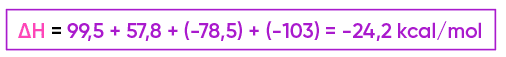
IV) Através da lei de Hess
A entalpia de uma reação pode ser calculada a partir da entalpia de outras reações, utilizando-se uma lei estabelecida pelo químico suíço G. H. Hess, em 1840: “para uma dada reação, a variação de entalpia é sempre a mesma, esteja essa reação ocorrendo em uma ou em várias etapas”.
Nesse tipo de problema, é dada uma série de equações que devem ser ajustadas para se chegar à equação final desejada. Para isso, podemos invertê-las, multiplicá-las ou dividi-las de forma conveniente para se chegar ao resultado desejado. Nesse caso, o DH também será multiplicado ou dividido (ou trocará de sinal, caso a equação tenha sido invertida). Veja no exemplo abaixo:
São dadas as equações termoquímicas:
I. C(grafite) + O2(g) ® CO2 (g) ΔH1 = -94,1 kcal
II. H2(g) + ½ O2(g) ® H2O(l) ΔH2 = -68,3 kcal
III. CH4(g) + 2 O2(g) ® CO2(g) + 2 H2O(l) ΔH3 = -212,8 kcal
Calcule o valor do ΔH da reação:
IV. C(grafite) + 2 H2(g) ® CH4(g) ΔH = ?
Observe que, na equação desejada, precisamos de 1 mol de C (grafite) nos reagentes (encontrada na equação I):
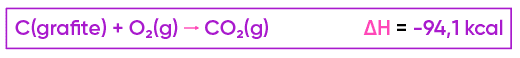
Também precisamos de 2 mols de H2(g) nos reagentes (encontrado na equação II, que deve ser multiplicada por 2):

E, finalmente, nos produtos, precisamos de 1 mol de CH4(g) (encontrado na equação III, que precisa ser invertida):

Somando-se agora essas 3 equações, chegamos ao resultado desejado 😉:
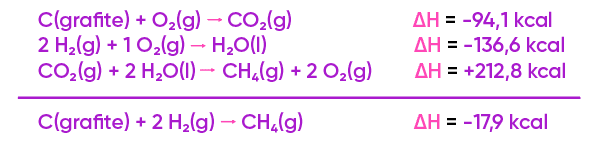
A Estequiometria na Termoquímica
Outro aspecto importante nas provas é a estequiometria nas reações termoquímicas. Pode-se calcular a energia liberada (ou absorvida) em uma reação a partir da quantidade das substâncias participantes, ou vice-versa. Veja o exemplo abaixo:
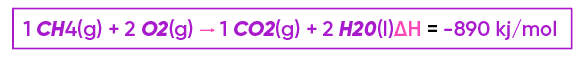
Podemos observar, nessa equação, que a queima de 1 mol de metano (CH4, 16 g/mol) é capaz de liberar 890 kJ de energia. Então, qual seria a quantidade de energia liberada na queima de 1 kg desse combustível? 🤔
Para responder, basta estabelecer uma proporção:
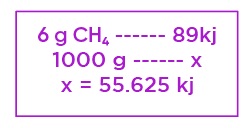
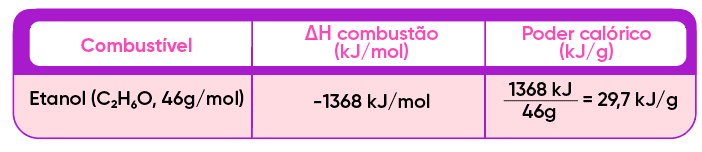
Já que estamos falando de combustíveis, é comum se observar a eficiência de um combustível a partir de seu poder calórico (a quantidade de energia liberada por unidade de massa, ou, às vezes, de volume da substância), como feito no exemplo anterior. Veja a tabela:

Isso é comum inclusive para os alimentos:

A conversão para unidade de volume é feita conhecendo-se a densidade do combustível (basta multiplicar o poder calorífico por massa pela densidade do combustível).
E isso é tudo, pessoal! Espero que vocês tenham gostado desse super conteúdo sobre Termoquímica para arrasar no Enem!
Afinal, este é um dos assuntos que mais caem em história no Enem!
Você quer ter acesso a mais conteúdo como este? Se sim, por que você não vem pro Explicaê?
Só aluno Explicaê Premium tem correções ilimitadas das suas redações por menos de R$1,35 por dia.
